D'Cyanogrupp huet eng staark Polaritéit an Elektroneabsorptioun, sou datt se déif an d'Zilprotein agoe kann fir Waasserstoffbrécke mat Schlësselaminosäurereschter am aktiven Zentrum ze bilden. Gläichzäiteg ass d'Cyanogrupp de bioelektroneschen isosteresche Kierper vu Carbonyl, Halogen an aner funktionelle Gruppen, wat d'Interaktioun tëscht klenge Medikamentemoleküle an Zilproteine verbessere kann, sou datt se wäit verbreet an der struktureller Modifikatioun vu Medikamenter a Pestiziden benotzt gëtt [1]. Déi representativ cyanohalteg medizinesch Medikamenter sinn Saxagliptin (Figur 1), Verapamil, Febuxostat, etc.; Landwirtschaftlech Medikamenter enthalen Bromofenitril, Fipronil, Fipronil a sou weider. Zousätzlech hunn Cyanoverbindungen och e wichtegen Uwendungswäert an de Beräicher Parfum, funktionelle Materialien a sou weider. Zum Beispill ass Citronitril en internationale neien Nitrilparfum, a 4-Brom-2,6-Difluorbenzonitril ass e wichtegt Rohmaterial fir d'Virbereedung vu Flëssegkristallmaterialien. Et kann een gesinn, datt Cyanoverbindungen a verschiddene Beräicher wéinst hiren eenzegaartegen Eegeschafte wäit verbreet benotzt ginn [2].
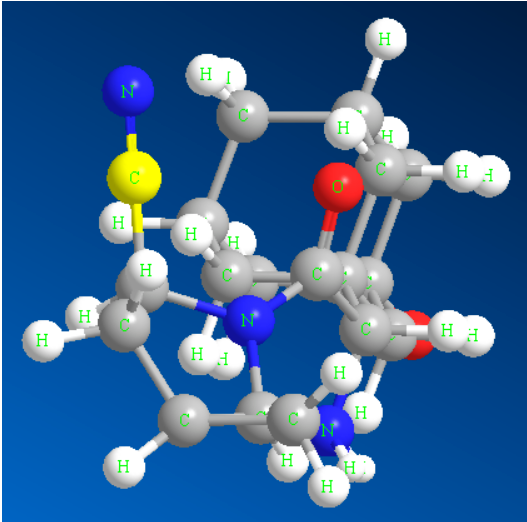
D'Cyanogrupp huet eng staark Polaritéit an Elektroneabsorptioun, sou datt se déif an d'Zilprotein agoe kann fir Waasserstoffbrécke mat Schlësselaminosäurereschter am aktiven Zentrum ze bilden. Gläichzäiteg ass d'Cyanogrupp de bioelektroneschen isosteresche Kierper vu Carbonyl, Halogen an aner funktionelle Gruppen, wat d'Interaktioun tëscht klenge Medikamentemoleküle an Zilproteine verbessere kann, sou datt se wäit verbreet an der struktureller Modifikatioun vu Medikamenter a Pestiziden benotzt gëtt [1]. Déi representativ cyanohalteg medizinesch Medikamenter sinn Saxagliptin (Figur 1), Verapamil, Febuxostat, etc.; Landwirtschaftlech Medikamenter enthalen Bromofenitril, Fipronil, Fipronil a sou weider. Zousätzlech hunn Cyanoverbindungen och e wichtegen Uwendungswäert an de Beräicher Parfum, funktionelle Materialien a sou weider. Zum Beispill ass Citronitril en internationale neien Nitrilparfum, a 4-Brom-2,6-Difluorbenzonitril ass e wichtegt Rohmaterial fir d'Virbereedung vu Flëssegkristallmaterialien. Et kann een gesinn, datt Cyanoverbindungen a verschiddene Beräicher wéinst hiren eenzegaartegen Eegeschafte wäit verbreet benotzt ginn [2].
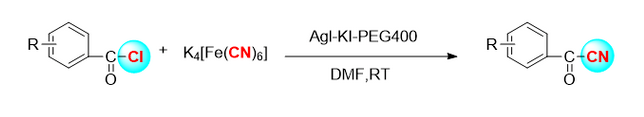
2.2 Elektrophil Zyanidéierungsreaktioun vun Enolborid
D'Team vum Kensuke Kiyokawa [4] huet d'Cyanidreagenzien n-Cyano-n-phenyl-p-toluolsulfonamid (NCTS) a p-Toluolsulfonylcyanid (tscn) benotzt fir eng héicheffizient elektrophil Zyanidéierung vun Enol-Borverbindungen z'erreechen (Figur 3). Duerch dëst neit Schema goufen verschidde β-Acetonitril a verschidde Substrater benotzt.
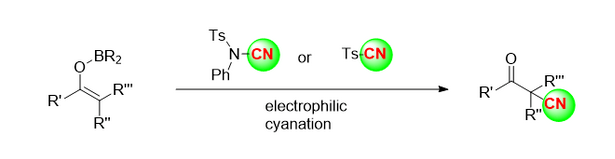
2.3 organesch katalytesch stereoselektiv Siliziumzyanidreaktioun vu Ketonen
Viru kuerzem huet d'Team vum Benjamin List [5] an der Zäitschrëft Nature d'enantiomer Differenzéierung vun 2-Butanon (Figur 4a) an déi asymmetresch Cyanidreaktioun vun 2-Butanon mat Enzymen, organesche Katalysatoren an Iwwergangsmetallkatalysatoren, mat Hëllef vun HCN oder tmscn als Cyanidreagens, publizéiert (Figur 4b). Mat tmscn als Cyanidreagens goufen 2-Butanon an eng breet Palette vun anere Ketonen ënner de katalytesche Konditioune vun idpi héich enantioselektive Silylcyanidreaktiounen ausgesat (Figur 4C).
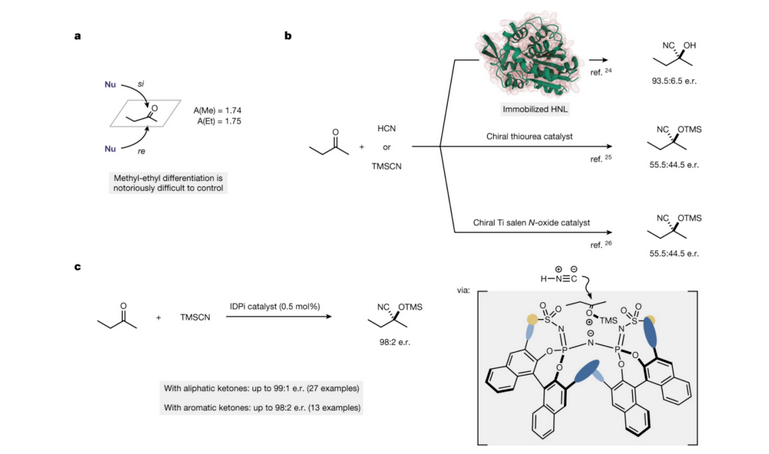
Figur 4 A, enantiomer Differenzéierung vun 2-Butanon. b. Asymmetresch Zyanidéierung vun 2-Butanon mat Enzymen, organesche Katalysatoren an Iwwergangsmetallkatalysatoren.
c. Idpi katalyséiert déi héich enantioselektiv Silylcyanidreaktioun vun 2-Butanon an enger breeder Palette vun anere Ketonen.
2.4 Reduktioun vun Zyanidéierung vun Aldehyden
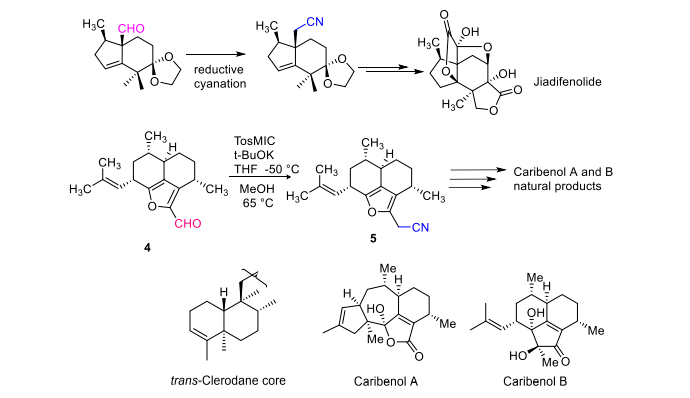
Bei der Synthese vun Naturprodukter gëtt dat gréngt Tosmik als Cyanidreagens benotzt, fir steresch gehënnert Aldehyder einfach an Nitriler ëmzewandelen. Dës Method gëtt weider benotzt, fir en zousätzlecht Kuelestoffatom an Aldehyder a Ketonen anzeféieren. Dës Method huet konstruktiv Bedeitung an der enantiospezifescher Gesamtsynthese vu Jiadifenolid an ass e Schlësselschrëtt an der Synthese vun Naturprodukter, wéi zum Beispill d'Synthese vun Naturprodukter wéi Clerodan, Caribenol A a Caribenol B [6] (Figur 5).
2.5 elektrochemesch Cyanidreaktioun vun organeschen Aminen
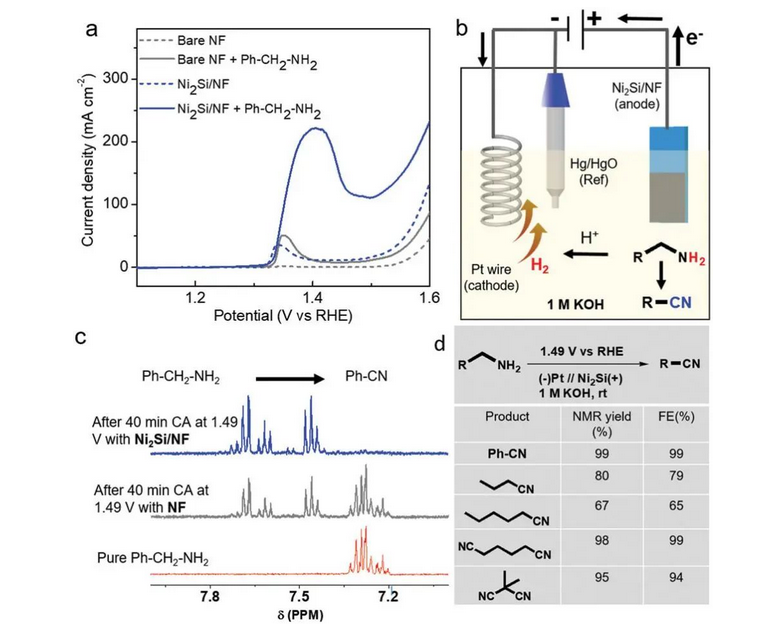
Als gréng Synthesetechnologie gëtt organesch elektrochemesch Synthese wäit verbreet a verschiddene Beräicher vun der organescher Synthese benotzt. An de leschte Jore hunn ëmmer méi Fuerscher sech drop konzentréiert. D'Team vum Prashanth W. Menezes [7] huet viru kuerzem bericht, datt aromatescht Amin oder aliphatescht Amin direkt zu entspriechende Cyanoverbindungen an 1m KOH-Léisung (ouni Zyanidreagens) mat engem konstante Potenzial vun 1,49vrhe mat engem bëllegen Ni2Si-Katalysator mat héijer Ausbezuelung oxidéiert ka ginn (Figur 6).
03 Zesummefassung
Zyanidéierung ass eng ganz wichteg organesch Synthesereaktioun. Ausgehend vun der Iddi vun der grénger Chimie ginn ëmweltfrëndlech Zyanidreagenzien agesat fir traditionell gëfteg a schiedlech Zyanidreagenzien z'ersetzen, an nei Methoden wéi lösungsmittelfräi, net-katalytesch a Mikrowellenbestrahlung ginn agesat fir den Ëmfang an d'Déift vun der Fuerschung weider auszebauen, fir grouss wirtschaftlech, sozial an ökologesch Virdeeler an der industrieller Produktioun ze generéieren [8]. Mam kontinuéierleche Fortschrëtt vun der wëssenschaftlecher Fuerschung wäert sech d'Zyanidreaktioun a Richtung héichrendement, wirtschaftlech a gréng Chimie entwéckelen.
Zäitpunkt vun der Verëffentlechung: 07.09.2022





